"液晶"を利用した温度応答性ドラッグデリバリーキャリアの創生 Design of thermoresponsive drug delivery carrier using "liquid crystal"
(2024年05月13日)

Contents
1.概要
-
本研究では,テレビやスマートフォンの画面に用いられている「液晶」の仕組みを利用したキラル液晶高分子ミセルによる温度応答性薬物キャリアを創出しました。
-
今回合成したキラル液晶高分子は,約49 ℃を境に液晶相から等方相へと転移することがわかりました。
-
このキラル液晶高分子は,水中で約150 nmのミセルを形成し,その内部に疎水性薬物を内包できることがわかりました。
-
キラル液晶高分子ミセルに内包したモデル薬物は,約49°C以下では,液晶高分子ミセル内に安定に保持されるのに対して,約49 °C以上ではミセルから放出されることがわかりました。
-
これまでに報告されている刺激応答性高分子ミセル型の薬物キャリアは,刺激に応答して内包薬物を瞬時に全て放出するものでしたが,今回合成したキラル液晶高分子ミセルは,従来のミセルとは全く異なり薬物放出のon-off制御ができること明らかにしました。
2.背景
ドラッグデリバリーシステム(DDS)とは,狙った場所に,狙ったタイミングで,必要な量だけ薬物を放出することにより,副作用を最小限に抑えて最大の薬効を発揮させるための技術です。これまでに,温度やpH,電場,生体分子などのさまざまな刺激に応答して薬物放出を制御するためのシステムが検討されてきました。特に,疎水性の薬物を内包できる高分子ミセルが精力的に研究されてきました。外部刺激に応答して疎水性から親水性へと変化する高分子を用いて高分子ミセルを調製すると,外部刺激に応答してミセルの形成と解離を制御できます。この刺激応答性ミセルに疎水性薬物を内包させると,刺激に応答したミセルの解離によって,薬物を放出することができます。しかし,この薬物放出はミセルの解離に基づいているため,刺激に応答して瞬時に内包した薬物を全て放出してしまいます。このように,従来の刺激応答性高分子ミセルでは,薬物放出量のコントロールが困難でした。
そこで宮田教授らは,テレビやスマートフォンの画面に用いられている「液晶」に着目しました。液晶は,固体のような規則的な構造と液体のような流動性を併せ持っており,温度や電場などの外部刺激に応答して,整列した状態から不規則な状態へと変化します。宮田教授はこれまでに,液晶高分子を用いて調製した膜が温度変化により引き起こされる液晶−等方相転移によって薬物透過を制御できることを見出していました。本研究では,高分子に液晶性を付与できるメソゲンにキラル構造を導入した両親媒性キラル液晶高分子を合成して,これを用いて調製した液晶高分子ミセルにより温度に応答した薬物のon-off制御を可能にしました。
3.成果
柔軟なポリシロキサン主鎖に疎水部として液晶構造を形成するためのキラル構造を有するメソゲン(キラルメソゲン)と,親水部として生体適合性に優れたオリゴエチレングリコール鎖を導入して両親媒性キラル液晶高分子を合成しました。
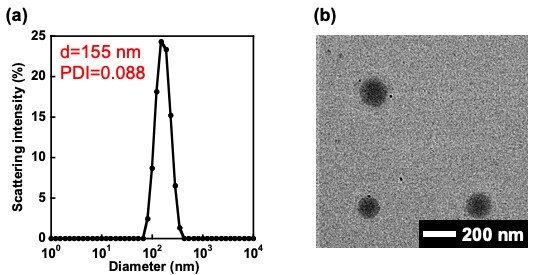
得られた両親媒性キラル液晶高分子の液晶−等方相転移温度(TNI)は約 49℃でした。また,得られた両親媒性キラル液晶高分子は水中で自己集合して,粒径が約150 nmのキラル液晶高分子ミセルを形成しました(図 1)。
このキラル液晶高分子ミセルは,加熱して液晶−等方相転移温度以上にしてもミセル構造が崩壊しないことがわかりました。このキラル液晶高分子ミセルにモデル薬物であるフルオレセインを内包させて温度変化によるフルオレセインの放出を評価したところ, T NI以下では薬物の放出がみられず, T NI以上において薬物が放出されることがわかりました。したがって,今回調製したキラル液晶高分子ミセルは従来の刺激応答性ミセルとは異なり,外部刺激に応答して薬物放出をon-off制御できることがわかりました(図 2)。
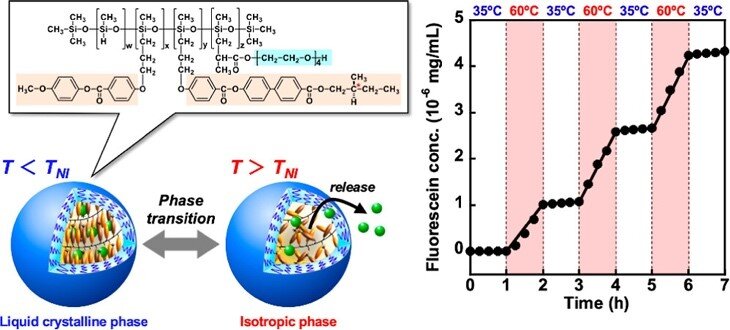
図2. キラル液晶高分子ミセルからの薬物放出制御
T NI 以下では規則構造を有する液晶相内で薬物の拡散が抑制されたのに対して,TNI以上では等方相へと変化して薬物の拡散性が著しく増加するためと考えられます。宮田教授らはこれまでに,液晶高分子ミセルによる薬物放出制御を試みていましたが,T NI 以下における薬物の漏出が課題でした。
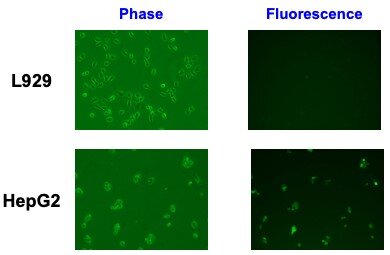
今回,メソゲンにキラル構造を導入することによって,より制御された規則構造を有する液晶相が形成されたことにより,TNI以下での薬物漏出が抑制されたと考えられます。また,非常に興味深いことに,キラル液晶高分子ミセルは,マウス線維芽細胞(L929)にはほとんど取り込まれないのに対して,ヒト肝がん由来細胞(HepG2)には取り込まれることがわかり,ガン由来細胞に対する特異性が期待できます(図3)。実用化までに乗り越えるべき課題は多くありますが,今回の研究成果は,液晶の医療応用という新しい応用展開につながるものであり,ますますの発展が期待できます。
4.論文情報
論文名:Reversible Regulation of Drug Release from Chiral Liquid Crystalline Polymer Micelles without Leakage (キラル液晶高分子ミセルを用いた可逆的な薬物放出制御)
著者名:Y Inoue , A Kawamura , and T Miyata.
雑誌名: Macromolecules
DOI: 10.1021/acs.macromol.3c01049
公表日:2023 年 10 月 5 日(オンライン公開)
◆著者プロフィール
河村暁文(化学生命工学部 化学・物質工学科 教授)
2008年大阪府立大学大学院工学研究科物質・化学系専攻学士課程後期課程修了,博士(工学)。化学生命工学部教授。2016年,高分子奨励賞,2023年日本接着学会学術賞。
◆研究室情報
先端高分子化学研究室 https://wps.itc.kansai-u.ac.jp/sentan/
生体界面材料研究室 https://wps.itc.kansai-u.ac.jp/kawamura/

